Begriffe wie „grüner Wasserstoff“, „Elektrolyse“ und „Wasserstoff-Elektrolyseur“ gewinnen zunehmend an Bedeutung. Wie wir in unserem jüngsten Blog über den Wasserstofftransport beschrieben haben, entstehen weltweit immer mehr Elektrolysesysteme, und viele Regierungen setzen auf die Einführung von grünem Wasserstoff als Teil des Übergangs zu erneuerbaren Energien.
Aber wie genau wird grüner Wasserstoff hergestellt? Was ist Elektrolyse, und was macht diese Technologie nachhaltig? In diesem Blog beantworten wir diese Fragen im Detail.
Grauer, blauer und grüner Wasserstoff
Obwohl wir den Unterschied zwischen grünem, blauem und grauem Wasserstoff bereits in unserem Blog über flüssigen Wasserstoff (LH2) ausführlich erörtert haben, möchten wir diese drei Produktionsverfahren noch einmal kurz erläutern.
Grauer Wasserstoff
Grauer Wasserstoff wird erzeugt durch Methandampfreformierung. Bei diesem Verfahren wird mit heißem Dampf Wasserstoff aus einer Methanquelle wie Kohle oder Erdgas erzeugt. Unter dem Druck von 3-25 bar reagieren die beiden Stoffe unter Zugabe eines Katalysators, und bei dieser Reaktion entstehen CO, CO2 und Wasserstoff.
Zur Herstellung von reinem Wasserstoff wird eine „Wasser-Gas-Shift-Reaktion“ erzeugt, bei der Wärme, CO und Wasserstoff entstehen. Die Herstellung von grauem Wasserstoff ist effizient, aber leider wegen der großen Menge an freigesetztem CO2 ziemlich umweltschädlich.
Blauer Wasserstoff
Eine nachhaltigere Alternative zu grauem Wasserstoff ist blauer Wasserstoff. Die Herstellung von blauem Wasserstoff funktioniert auf die gleiche Weise wie die von grauem Wasserstoff, aber bei dieser Methode wird der größte Teil des CO2 abgefangen, gespeichert oder wiederverwendet. Das macht das Verfahren deutlich nachhaltiger, aber auch teurer, da die Infrastrukturen zur Abscheidung des freigesetzten CO2 einen hohen Material- und Energieaufwand erfordern.
Grüner Wasserstoff
Während grauer und blauer Wasserstoff durch Methandampfreformierung erzeugt wird, wird grüner Wasserstoff durch Elektrolyse hergestellt. Bei diesem Herstellungsverfahren wird kein CO2 freigesetzt, so dass grüner Wasserstoff als nachhaltiger Kraftstoff und Energieträger der Zukunft gilt.

Was ist ein Elektrolyseur für Wasserstoff?
Was ist ein Elektrolyseur für Wasserstoff?
Elektrolyse ist einfach eine chemische Reaktion, bei der Elektrizität verwendet wird, um zusammengesetzte Stoffe in einzelne oder zusammengesetzte Stoffe aufzuspalten.
Diese Methode kann auf eine Vielzahl von Stoffen angewendet werden, ist aber derzeit am besten für die Spaltung von Wasser zur Erzeugung von Wasserstoff bekannt. Die Elektrolyse von Wasser wurde bereits 1807 von Humphry Davy entdeckt, der seine Erkenntnisse noch im selben Jahr der Royal Society of London vorstellte.
Bei der Wasserelektrolyse wird Wasser mit Hilfe elektrischer Energie in Wasserstoff und Sauerstoff gespalten. Der Sauerstoff wird entweder bei dem Prozess freigesetzt oder abgefangen und genutzt; der Wasserstoff kann mit Hilfe eines Verflüssigers in flüssigen Wasserstoff (LH2) umgewandelt werden oder nicht.
Der Elektrolyseur ist eine umgekehrte Brennstoffzelle. Eine Brennstoffzelle erzeugt Strom, indem sie Wasserstoff mit Sauerstoff kombiniert, während die Elektrolyse Strom verwendet, um Wasserstoff und Sauerstoff zu produzieren.
Wie funktioniert das? Ein Elektrolysesystem besteht aus einem Wasserbehälter mit einem Elektrolyt und zwei Elektroden: einer Kathode (negativer Pol) und einer Anode (positiver Pol). Auf beiden Seiten des Elektrolyten findet eine chemische Reaktion statt, indem elektrischer Strom an beide Elektroden geleitet wird. Auf der Kathodenseite wird Wasserstoff freigesetzt, auf der Anodenseite Sauerstoff.
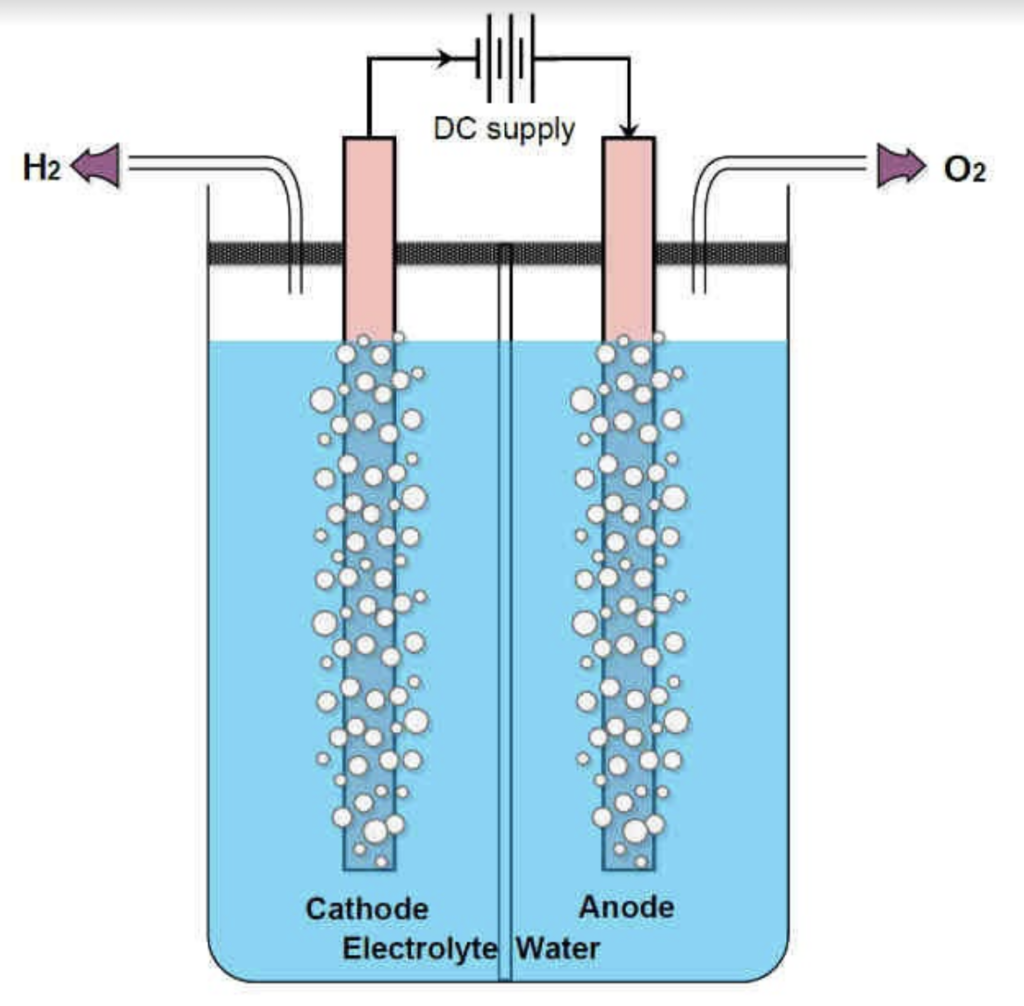
Quelle: International Journal of Engineering and Advanced Technology (IJEAT)
Natürlich muss der Elektrolyseprozess mit nachhaltig erzeugter Energie betrieben werden, z. B. mit Sonnenenergie, Windenergie, Wasserkraft oder Biomasse. Ist dies nicht der Fall, ist die Elektrolyse zwar immer noch möglich, aber sie kann dann nicht als nachhaltiger grüner Wasserstoff bezeichnet werden.
Zwei Arten von Elektrolyseuren
Das Prinzip der Elektrolyse ist gut bekannt, aber es gibt verschiedene Arten von Elektrolyseuren. Die beiden bekanntesten Elektrolyseure für Wasserstoff sind der alkalische Elektrolyseur und der PEM-Elektrolyseur.
Der alkalische Elektrolyseur
Der alkalische Elektrolyseur verwendet einen flüssigen alkalischen Elektrolyten. Das Wasser in diesem Elektrolyten wird am Kathodenpol in Wasserstoff- und Hydroxidionen aufgespalten. Diese Ionen werden dann mit einer Membran in Kontakt gebracht, woraufhin sie am Anodenpol zu Wasser und Sauerstoff oxidiert werden.
Sowohl an der Kathode als auch an der Anode findet eine chemische Reaktion statt:
Kathode: 2 H2O + 2e → H2+ 2 OH-
Anode: 2 OH- → ½ O2+ 2e- + H2O
Gesamtreaktion: H2O → H2+ ½ O2.
Zur Einleitung dieser Reaktion sind etwa 285 kJ/mol erneuerbare Energie erforderlich (etwa 50 KJ/mol Wärme und 235 kJ/mol erneuerbare Elektrizität pro Mol Wasser). Die Temperatur, bei der die Elektrolyse stattfindet, liegt zwischen 40 und 90 °C.
Elektrolyseure, die flüssige alkalische Natrium- oder Kaliumhydroxidlösung als Elektrolyt verwenden, sind seit langem verfügbar und haben sich für die Wasserstofferzeugung bewährt. Zu den Nachteilen dieser Methode gehören jedoch die relativ geringe Energiedichte der Zellen und die Tatsache, dass die Zellen nicht unter hohem Druck arbeiten können und daher recht groß sind.
Der PEM-Elektrolyseur
Ein PEM-Elektrolyseur verwendet eine Polymermembran, die nur Wasserstoffionen durchlässt. Das Wasser wird an der Anode in Sauerstoff, Wasserstoffionen und zwei Elektronen gespalten. Die Wasserstoffionen und die beiden Elektronen passieren dann die Membran und werden an der Kathode in Wasserstoff umgewandelt.
Sowohl an der Kathode als auch an der Anode findet eine chemische Reaktion statt:
Anode: H2O → H2+ ½ O2+2e
Kathode: 2H+ + 2e → H2
Ein Vorteil des PEM-Elektrolyseurs gegenüber dem alkalischen Elektrolyseur ist die Tatsache, dass er auch unter Druck funktioniert und daher kleiner sein kann. Allerdings hat diese Methode auch Nachteile. So arbeitet der PEM-Elektrolyseur unter stark säurehaltigen Bedingungen, was besondere Anforderungen an das System stellt.
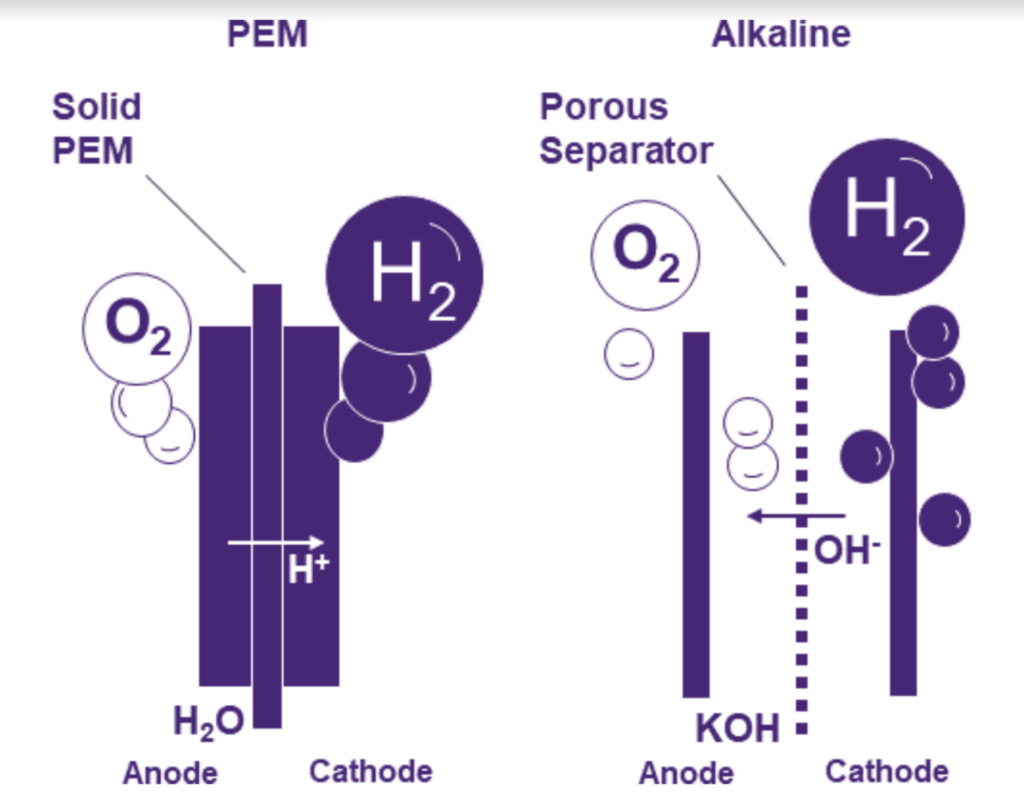
Quelle: Siemens
Möchten Sie mehr wissen?
Demaco arbeitet seit Jahrzehnten an den besten Infrastrukturen für Flüssigwasserstoff (LH2) und entwickelt und produziert vakuumisolierte Transferleitungen und verschiedene Hilfsprodukte. Demaco führt auch Projekte für den Transport, die Speicherung und die Anwendung von flüssigem Wasserstoff durch.
Wenn Sie Fragen zu unserer Branche haben, zögern Sie bitte nicht, uns zu kontaktieren. Oder schauen Sie sich unsere Produkte und Projekte an, um weitere Informationen zu erhalten.
Möchten Sie mehr über flüssigen Wasserstoff (LH2) erfahren? Dann werfen Sie einen Blick auf diese Seite oder lesen Sie unseren aktuellen Blog zum Thema „Wozu wird Wasserstoff verwendet?“. Lesen Sie hier alles über diese vielseitige kryogene Flüssigkeit und die langjährigen Erfahrungen, die Demaco in verschiedenen hochmodernen Wasserstoffprojekten gesammelt hat.

